Прогноз для пациентов с метастатическим раком молочной железы (мРМЖ) варьирует и зависит от множества факторов: возраста, статуса по HR и HER2, наличия висцеральных
метастазов в печень и/или легкие, времени без развития метастазов, работоспособности пациента и др.1–3 . Известно также, что эффективность предшествующего лечения существенно влияет на результативность последующих линий терапии мРМЖ4.
Был проведен анализ данных представляющих особый клинический интерес пациентов с худшим по сравнению с общей популяцией прогнозом, участвовавших в исследовании фазы IIIb CompLEEment-15. В этом исследовании изучается безопасность и эффективность ингибитора циклин-зависимых киназ 4/6 (CDK4/6) рибоциклиба в комбинации с летрозолом в большой группе пациентов6.
Основные выводы исследования5.
- Во всех подгруппах с менее благоприятным прогнозом по сравнению с общей популяцией прогнозом была показана клинически значимая эффективность лечения.
- Частота клинической эффективности в подгруппах составила 57.6-62.4%, что подтверждает эффективность рибоциклиба в лечении пациентов с предшествующей химиотерапией, висцеральными метастазами и ECOG 2.
- Профиль безопасности был ожидаемым и управляемым, наблюдались низкие показатели прекращения приема препарата из-за нежелательных явлений (НЯ).
- В подгруппах с ECOG 2 с висцеральными метастазами и без них наблюдалось меньше связанных с лечением НЯ степени ≥3 по сравнению с общей популяцией.
Дизайн исследования.
Рисунок 1. Дизайн исследования

ПБПЗ – период без признаков заболевания, ГТ – гормональная терапия, НСИА – нестероидные ингибиторы ароматазы, ФС – функциональный статус, ECOG
(Eastern Cooperative Oncology Group) – Восточная объединенная группа онкологов, РИБ – рибоциклиб, ЛЕТ – летрозол, ВДП – время до прогрессирования, ЧОО – частота объективных ответов, ЧКЭ – частота клинической эффективности.
В качестве подгрупп пациентов, представляющих особый клинический интерес были выбраны пациенты:
- С предшествующей химиотерапией по поводу мРМЖ (пХТ);
- ECOG 2;
- С висцеральными метастазами и предшествующей химиотерапией (ВМ+пХТ);
- С висцеральными метастазами и ECOG 2 (ВМ+ECOG 2).
Результаты8
Как и ожидалось, время до прогрессирования (ВДП) у пациентов в исследуемых подгруппах было короче, чем в общей популяции (Рисунок 2). В целом, пациенты с ВМ и пХТ или ECOG 2 имели худший прогноз в отношении ВДП, чем пациенты только с ВМ (22.9 месяца, диапазон 22.0-25.0 месяцев). В то же время эффективность лечения в отношении частоты общего ответа (ЧОО) и частоты клинической пользы (ЧКП) наблюдались во всех подгруппах (Рисунок 3). Согласно проведенному анализу, профиль безопасности в подгруппах пХТ и
ВМ+пХТ согласуется с профилем безопасности для общей популяции. Частоты НЯ были сопоставимы в подгруппах ECOG 2 и ВМ+ECOG 2, а также в общей когорте пациентов. Частота НЯ степени ≥3, а также серьезных НЯ степени ≥3, как правило, была выше, чем в общей популяции. Тем не менее, частота связанных с лечением НЯ всех степеней и степени ≥3 была ниже, чем в общей популяции (Рисунок 4). Частота прекращения лечения, связанного с НЯ любой степени и степени ≥3, в изученных подгруппах пациентов была ниже по сравнению с общей популяцией.
Наиболее частыми НЯ во всех подгруппах были нейтропения (62.3-74.7%) и тошнота (33.5-49.4%). Удлинение интервала QT было нечастым во всех подгруппах, однако частота удлинения интервала QT любой степени и степени ≥3 была выше во всех подгруппах по сравнению с общей популяцией (Рисунок 5).
Рисунок 2. ВДП в подгруппах.
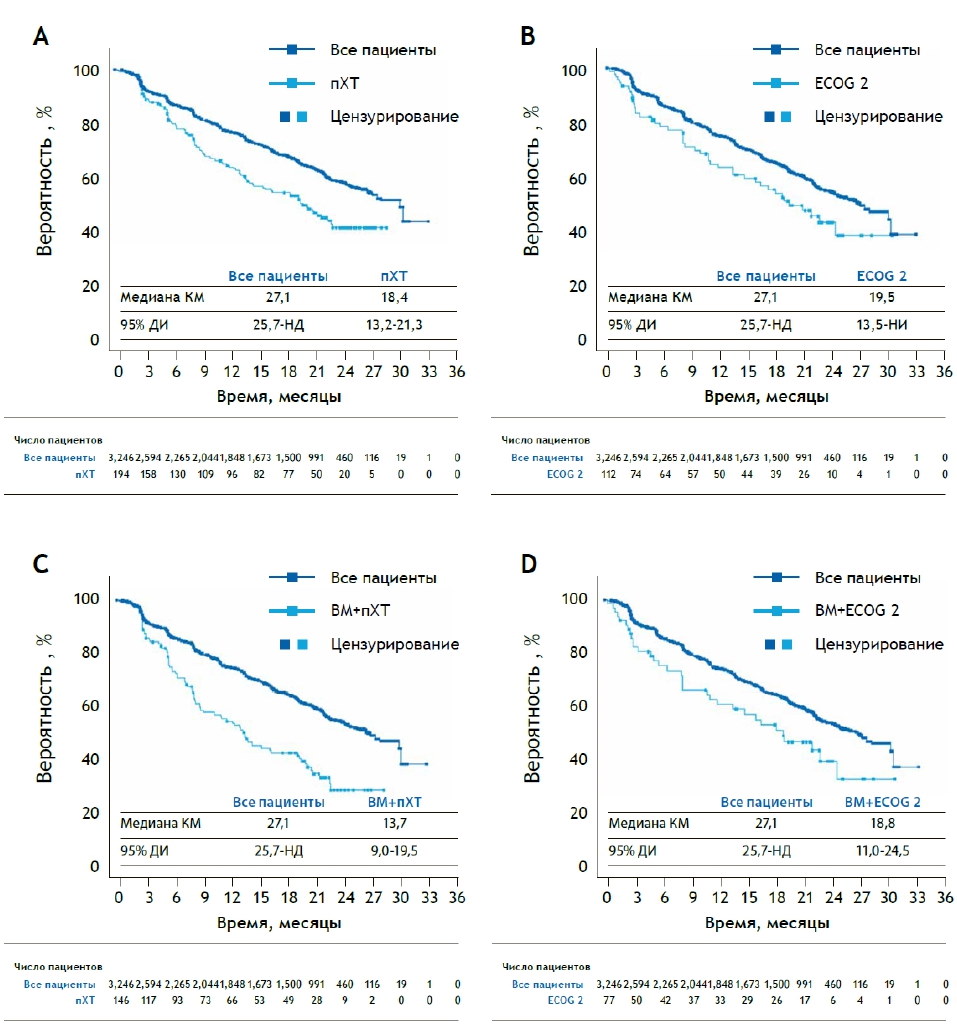
КМ — Каплан-Майер; НД — не достигнуто, НИ — не измеримо
Рисунок 3. Показатели эффективности в подгруппах для пациентов с поддающимся измерению заболеванием исходно.
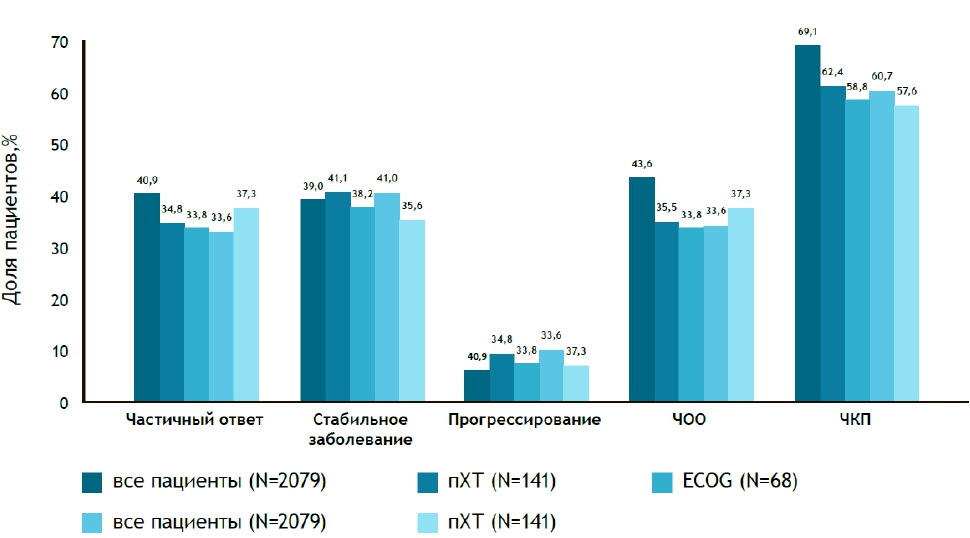
ЧОО — частота объективного ответа, ЧКП — частота клинической эффективности
* Частота полного ответа составила 2,7% в общей популяции, 0,7% в подгруппе пХТ и 0,8% в подгруппе ВМ+пХТ
Рисунок 4. Частоты связанных с лечением НЯ в подгруппах и в общей популяции пациентов.
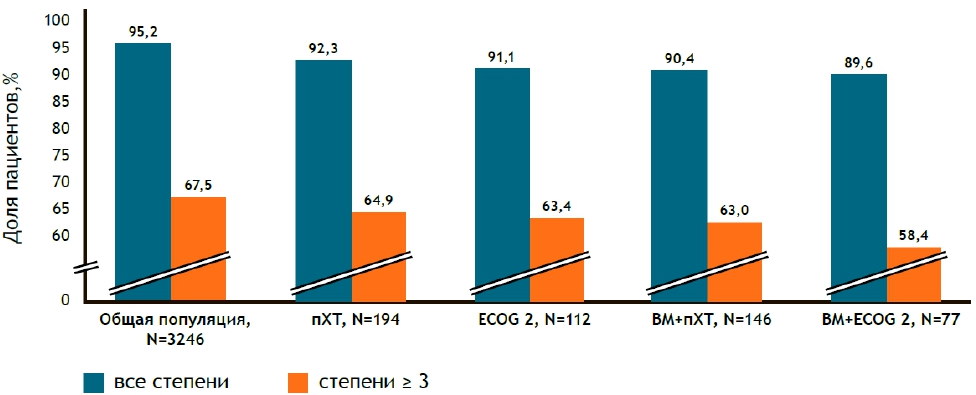
Рисунок 5. Частоты удлинения интервала QT в подгруппах
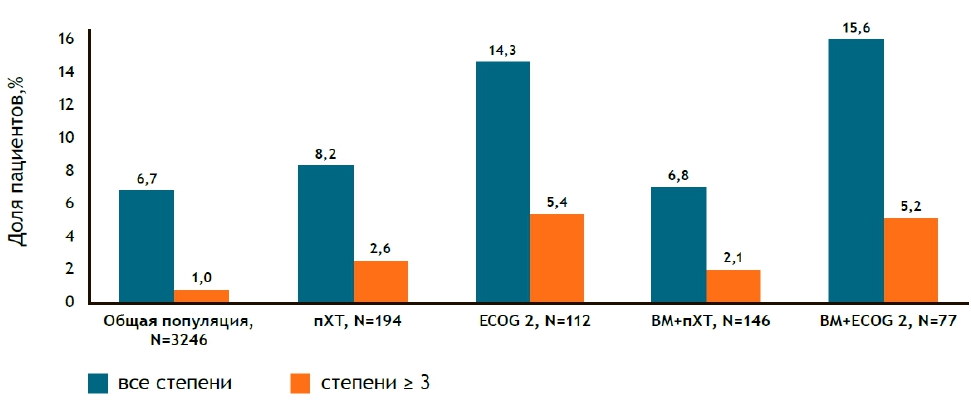
Список литературы
- Kazmi S, Chatterjee D, Raju D, Hauser R, Kaufman PA. Overall survival analysis in patients with metastatic breast cancer and liver or lung metastases treated with eribulin, gemcitabine, or
capecitabine. Breast Cancer Res Treat. 2020;184(2):559-565. doi:10.1007/s10549-020-05867-0 - Lobbezoo DJA, Van Kampen RJW, Voogd AC, et al. Prognosis of metastatic breast cancer: Are there differences between patients with de novo and recurrent metastatic breast cancer? Br J Cancer. 2015;112(9):1445-1451. doi:10.1038/bjc.2015.127
- Karakaya S, Karadağ İ, Duran AO, Oksuzoglu OB, Demirci U. Clinical outcomes and prognostic factors in HER-2 positive breast cancer with brain metastasis: A single-center experience. J Clin Oncol. 2020;38(15_suppl):e13015-e13015. doi:10.1200/jco.2020.38.15_suppl.e13015
- Park IH, Lee KS, Ro J. Effects of second and subsequent lines of chemotherapy for metastatic breast cancer. Clin Breast Cancer. 2015;15(1):e55-e62. doi:10.1016/j.clbc.2014.09.001
- Cottu PH, Ring A, Marchetti P, et al. Ribociclib (RIB) + letrozole (LET) in subgroups of special clinical interest with hormone receptor-positive (HR+), human epidermal growth factor receptor 2-negative (HER2–) advanced breast cancer (ABC): Subgroup analysis from the CompLEEment-1 trial. Ann Oncol. 2020;31:S379-S380. doi:10.1016/j.annonc.2020.08.435
- DeLaurentiis M, Borstnar S, Campone M, et al. Interim results from the full population of the phase 3b CompLEEment-1 study of ribociclib (RIBO) plus letrozole (LET) in the treatment of HR+/HER2– advanced breast cancer (ABC). J Clin Oncol. 2019;37(15_suppl):1041-1041. doi:10.1200/jco.2019.37.15_suppl.1041
Безопасность пациента является наивысшим приоритетом для компании «Новартис». Если у Вашего пациента развилось нежелательное явление на фоне приема препарата производства компании «Новартис», Вы можете сообщить о нем в компанию «Новартис Фарма» по телефону +7 495 967 12 70 или отправить сообщение на электронный адрес: drug.safety_russia@novartis.com. Сообщение предназначено только для медицинских и фармацевтических работников.
268707/abc/digita/07.21/0

